EMPACTA
 【論文】
【論文】
Salama C, Han J, Yau L, Reiss WG, et al.
Tocilizumab in Patients Hospitalized with Covid-19 Pneumonia. N Engl J Med. 2021 Jan 7;384(1):20-30. doi: 10.1056/NEJMoa2030340. Epub 2020 Dec 17. PMID: 33332779; PMCID: PMC7781101.
【Reviewer】
Taisuke Shibata, Eri Kobayashi
【Summary】
良くデザインされた多施設二重盲検RCTによって、人工呼吸器管理の必要ない、covid-19肺炎入院患者に対して、standard of care(抗ウイルス薬、ステロイド、その他対症療法)+Tocilizumabの投与は、 Standard of care + プラセボに比較して、 人工呼吸器やECMOの導入率、または、死亡率の複合outcomeを改善した。
非人工呼吸器管理の患者に使用することは、重症化を防ぐという意味で使用する意義がありそうである。
【わかっていること】
- Covid-19肺炎は、人工呼吸器管理を要することがあり、特に65歳以上の場合に死亡率が上昇する
- 治療は、全身管理と対症療法だが、remdesivirがアメリカでは認可されている治療法であり、 その他、dexamethasoneが唯一死亡率を下げる治療法であることがわかっている1)。
- IL-6の値は、Covid-19の重症度と正の相関関係があり、人工呼吸器管理の予測因子となる可能性が示唆されている。
- Tocilizumabは、抗IL-6受容体抗体であり、アメリカの観察研究ではCovid-19肺炎の患者の予後を改善したという観察研究がある 2-4)。
【わかっていないこと】
- 人工呼吸器管理されていない、Covid-19肺炎の入院患者に対するTocilizumabの安全性と有効性は、確立されていない
【仮説/目的】
人工呼吸器管理されていないCovid-19肺炎の入院患者に対して、 Tocilizumabの使用は、人工呼吸器やECMO導入に至るリスクを減らす。
【PICO】
P: 人工呼吸器管理されていない、18歳以上のCovid-19肺炎の入院患者
I: Tocilizumab 8mg/kgを生理食塩水100mLに溶解して、1回または2回投与
C: 生理食塩水100mLを1回または2回投与
O: Primary:28日時点での人工呼吸器、ECMOの使用率、または死亡率
Method
【期間】 2020/5/14 〜 2020/8/18
【場所】 アメリカを中心としたmulti-center trial
【デザイン】 多施設二重盲検RCT
- 事前プロトコルの有無: あり
- ランダム化の方法:
・permuted blockランダム化を用いて、介入群:対照群を2:1で割り付け。
・また、60歳未満と60歳以上で層別ランダム化も用いている - 割付隠蔽化の有無:
・対話型音声システム、またはwebに基づいた割り付けシステム(IxRS)で割り付けしているため、コンシールメントされている - マスキングの有無、その対象:
・ 患者、試験施設職員(薬剤師を除く)は、マスキングされているため二重盲検化できている
・ 薬剤提供者も、一部の役割を除いて盲検化されている
・ このプロジェクトチームも、統計学者も盲検化されている
・ 内部モニタリング委員会は、盲検化されていない
【患者選択基準】
Inclusion Criteria:
- 18歳以上の入院患者
- Covid-19のPCR検査陽性(咽頭、血液、尿、便、その他の体液を検体とする)
- 胸部レントゲンもしくはCTでCovid-19肺炎像を呈している
- study protocolを完遂できると調査者が判断したもの
- 入院後96時間以内に 、スクリーニングが完了できる
- 室内気でSpO2 94%以下
- 最終薬剤投与から90日間、性交渉を控えるまたは避妊をすることに同意する妊孕性のある女性
- 最終薬剤投与から60日間、性交渉を控えるまたは避妊をすることに同意する男性
Exclusion Criteria:
- Tocilizumabまたはその他のモノクローナル抗体に重度のアレルギー症状の既往がある患者
- CPAP、BIPAP、人工呼吸器の装着の必要性がある患者
- 活動性結核、またはランダム化1ヶ月以内の結核感染の既往がある患者
- 活動性の細菌、真菌、ウイルス、その他の感染の疑いがある(HIVなど)患者
- 調査者の見解で、治療介入をしても24時間以上の余命が見込まれない患者
- HIVなど免疫不全がある患者、免疫抑制療法を受けている患者 (ただし、Covid-19に対するステロイド投与は除く)
- 3ヶ月以内に、経口免疫抑制薬やTocilizumabを含む免疫賦活薬の治療を受けている患者
- 他のIL-6アンタゴニストやその他の臨床試験に参加している患者
(ただし、Medical Monitorによって許可されているCovid-19の抗ウイルス薬の臨床試験に参加している患者は参加可能) - スクリーニングから24時間以内に測定されたAST,ALTが正常上限の5倍以上の患者
- スクリーニング時点で、ANC<1000/μLの患者
- スクリーニング時点で、血小板<50000μLの患者 ・妊娠中、授乳中、妊娠検査陽性の患者
- 憩室炎や胃穿孔の既往がある患者
※remdesivir, hydroxychloroquine, chloroquineを使用していても参加可能。 Primary medical teamに判断を委ねられる
【介入】
- Tocilizumabは、静脈注射剤として10mL入り(200mg /10mL)または20mL入り(400mg /20mL)のガラスバイアルを供給される。
- Tocilizumab 8mg/kgを生理食塩水に溶解して総量100mLにして点滴静注。最大800mg。
- 臨床症状の増悪(発熱の遷延、7段階スケールで1段階以上の増悪)見られた場合には、1回目の投与から8〜24時間以上空けて、同量を追加で投与する。その後は追加投与できない。
【対照】
- 生理食塩水100mLを静注。
- 0.9%塩化ナトリウム(生理食塩水)の袋に入れて治験施設から供給される。
- 介入群と同様に1回の追加投与可能。
【両群共通のプラクティス】
- 両群ともに、standard of careを受けられる(抗ウイルス薬、ステロイド投与、対症療法)
- Chloroquine、Hydroxychloroquineは、最大400mg1日2回までなら可能
- methylprednisolone 1mg/kg以下、またはそれに値するステロイド投与を5日以内であれば可能
- 酸素投与、解熱鎮痛薬、抗アレルギー薬、気管支拡張薬などの対症療法は可能
- 以下、併用禁止治療
→・ Covid-19に対する抗ウイルス薬以外の現在臨床試験中の薬物
・細胞障害性治療
・生物学的製剤(sarilumab, siltuximabを含むIL-6/IL-6受容体治療、 TNFアンタゴニスト)
・JAK阻害薬(tofacitinib, baricitinib)
・アルキル化製剤(chlorambucil, cyclophosphamide)
・thalidomide、ガンマグロブリン、抗胸腺細胞グロブリン、azathioprine
・骨髄移植後の放射線全照射
・血漿交換
・研究期間中の生ワクチン不活化ワクチン接種
【主要評価項目】
- 28日時点での人工呼吸器、ECMOの使用率、または死亡率
【副次評価項目】
- 7段階評価スケールにおいて、2段階以上の改善を認めるまでの期間
- 治療失敗(死亡、人工呼吸器管理、ICU入室、使用中止)に至るまでの期間
- 28日時点での死亡率
- 退院、または退院の準備ができた状態(社会調整待ち)に至るまでの期間
【解析計画】
- 目標N; 253 + 126 = 379人
- サンプルサイズ計算
α= 5%, Power (1-β)= 80%, 対照群のアウトカム= 40%, 介入群のアウトカム= 25%
ARR= 15% - 検定方法: log-rank検定
- ITTの有無: あり
Results
【結果】
- フローダイアグラムの解釈(フォローアップ率、除外理由)
フォローアップ率:介入群90.4%、対照群 89.8%
脱落理由:
- 患者自身でのwithdraw
- Tocilizumabを投与したのか
- 確認が取れない
- 治療のアドヒアランス
治療完遂率が、介入群90.4%、対照群89.8%であり、アドヒアランスは高いと言える - 主要評価項目
介入群12.0%(95%CI 8.5〜16.9)、対照群19.3%(95%CI 13.3〜27.4)で、HR 0.56(95%CI 0.33〜0.97, P=0.04) - 副次評価項目
臨床的失敗までの期間の中央値は、HR0.55(95%CI 0.33〜0.93)
28日以内の退院、またその準備ができ他状態に至るまでの期間の中央値は、介入群6.0日(95%CI 6.0〜7.0日)、対照群7.5日(95%CI 7.0〜9.0日)で、HR 1.16(95%CI 0.91〜1.48)
臨床的な患者の状態の改善までの期間の中央値は、介入群6.0日(95%CI 6.0〜7.0日)、対照群7.0日(95%CI 6.0〜9.0日)で、HR1.15(95%CI 0.90〜1.48)
死亡は、介入群で26人(10.4% 95%CI 7.2〜14.9)、対照群で11人(8.6% 95%CI 4.9〜14.7)(weighted difference, 2.0 percentage points; 95% CI, -5.2 to 7.8)
結果の総括
- 本研究では両群ともに50%以上が抗ウイルス薬またはステロイドを使用している。 使用している患者の割合は両群で均等なので、純粋にTocilizumabの効果を評価できている。 その上で、過去の研究に比較して、退院までの日数の中央値が大幅に改善している。 これは、過去研究と比較して、抗ウイルス薬またはステロイドの使用率が高いことが可能性として考えられる。
(COVACTAは、Glucocorticoidsの使用が20%前後、抗ウイルス薬が25%前後の使用) 5)
COVACTA → 介入群:20日、対照群:28日
本研究 → 介入群:6.0日、対照群:7.5日 - 人工呼吸器装着 or 死亡率の複合Outcomeでは有意差を認めるものもあるが、 死亡率を改善するというstudyはない。
- 本研究も、複合Outcomeでは有意差を認めたものの、死亡率の改善には至らなかった。
- Sub group解析による人種または民族に応じて評価されたPrimary outcomeの結果は、全患者集団における結果と一致していた。
【著者の結論】
人工呼吸器管理の必要ない、Covid-19肺炎入院患者に対して、Standard of care(抗ウイルス薬、ステロイド、その他対症療法)+Tocilizumabの投与は、 Standard of care + プラセボに比較して、 人工呼吸器やECMOの導入率、または、死亡率の複合outcomeの改善に有用である。
----------------------------
論文の解釈
【論文の結論】
- 飛躍していないか
飛躍していない
【批判的吟味】
<内的妥当性>
Strength
- 二重盲検化されている
- RCTであることから、交絡因子は排除されている
- 完遂率が両群ともに90%前後であることから、結果の妥当性は高い
- 対話型音声システム、またはwebに基づいた割り付けシステム(IxRS)を利用して割り付けしており、割り付け者に十分なコンシールメントができている
- 7段階スケールは、客観的な指標となっており、評価しやすい
Limitation
- 人工呼吸器の明確な導入基準が定められていない
- ICU入室の明確な基準が定められていない
<外的妥当性>
Strength
- 多施設研究
- 年齢は、60歳未満が6割、60歳以上が4割であり、多くの年齢層に幅広く適応できる
Limitation
- subgroup解析では、どの人種でも同様の結果にはなっているものの、アジア人の比率が小さく そのまま日本人には適応しにくい
- 薬剤投与量は理想体重で計算されているものの、 BMI 32.4±7.6で日本人離れしている。
【Implication】
- 非人工呼吸器管理のCovid-19肺炎入院患者に対して、Tocilizumabを投与することは、
・ 人工呼吸器やECMO導入率または死亡率の複合outcomeを改善させる可能性がある
・ 投与することによって有害事象が顕著に増加することはなさそう
→非人工呼吸器管理の患者に使用することは、重症化を防ぐという意味で使用する意義はある。 日本人は本論文のpopulationとは体格が大きく異なるため、薬物の投与量には注意が必要。 ただ、挿管患者など重症例に有効かどうかは本論文では不明。今後の研究が待たれる。
参考:Tocilizumabに関する研究
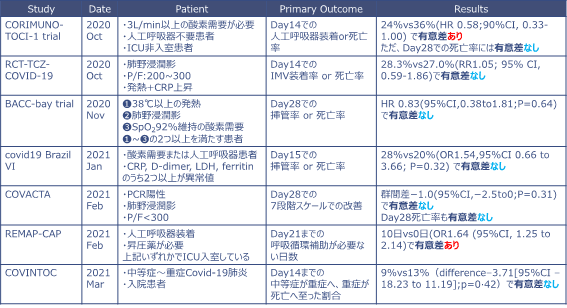
【本文サイト】https://www.nejm.org/doi/full/10.1056/NEJMoa2030340
【もっとひといき】トシリズマブをレビュー:https://www.kameda.com/pr/intensive_care_medicine/post_60.html
【引用】
1) The RECOVERY Collaborative Group. Dexamethasone in hospitalized patients with Covid-19 -- preliminary report. N Engl J Med. DOI: 10.1056/NEJMoa2021436.
2) Aziz M, Fatima R, Assaly R. Elevated interleukin-6 and severe COVID-19: a meta- analysis. J Med Virol 2020;92:2283-5.
3) Zhu J, Pang J, Ji P, et al. Elevated inter- leukin-6 is associated with severity of COVID-19: a meta-analysis. J Med Virol 2020 May 29 (Epub ahead of print).
4) Herold T, Jurinovic V, Arnreich C, et al. Elevated levels of IL-6 and CRP predict the need for mechanical ventilation in COVID- 19. J Allergy Clin Immunol 2020;146(1): 128-136.e4.
5) Ivan O Rosas , Norbert B, Michael W, et al. Tocilizumab in Hospitalized Patients with Severe Covid-19 Pneumonia. N Engl J Med. 2021 Apr 22;384(16):1503-1516.
このサイトの監修者
 亀田総合病院
亀田総合病院
集中治療科部長 林 淑朗
【専門分野】
集中治療医学、麻酔科学

